Константа равновесия химической реакции. Химическое равновесие: константа химического равновесия и способы ее выражения Константа химического равновесия не зависит от
Химическое равновесие – состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости в каждой паре прямая-обратная реакция равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем
А2 + В2 ⇄ 2AB
Количественной характеристикой химического равновесия служит величина, называемая константой химического равновесия.
При постоянной температуре константа равновесия обратимой реакции представляет собой постоянную величину, показывающую то соотношение между концентрациями продуктов реакций и исходных веществ, которая устанавливается при равновесии.
Уравнение константы равновесия показывает, что в условиях равновесия концентрации всех веществ, участвующих в реакции связаны между собой. Изменение концентрации любого из этих веществ влечёт за собой изменение концентрации всех остальных веществ. В итоге устанавливается новая концентрация, но соотношение между ними отвечает константе равновесия.
58. Факторы, определяющие направление протекания химических реакций. Химические процессы должны протекать в направлении уменьшения внутренней энергии системы, т.е. в направлении, отвечающему положительному тепловому эффекту реакции.
Вторым фактором, влияющим на направленность химических реакций является принцип направленности процессов наиболее вероятному состоянию, т.е. при химических реакциях, в силу принципа направленности процессов минимуму внутренней энергии, атомы соединяясь в молекулы, при образовании которых выделяется наибольшее количество энергии.
Тенденция к переходу в состояние с наименьшей внутренней энергией проявляется при температуре в одинаковой степени. Тенденция к достижению наиболее вероятного состояния проявляется тем сильнее, чем выше температура. При низких температурах в большинстве случаев практически сказываются только влияние первой из этих тенденций, в результате чего самопроизвольно протекают экзотермические процессы. По мере возрастания температуры равновесие в химических системах всё больше и больше сдвигается в сторону реакции разложения или увеличения числа состояний атомов. При этом каждой температуре отвечает состояние равновесия, характеризующееся определённым соотношением концентрации реагирующих веществ и продуктов реакции
59. Смещение химического равновесия. Принцип Ля Шателье. Если система находится в состоянии равновесия, то она будет пребывать в нём до тех пор, пока внешние условия сохраняются постоянными. Наибольшее значение имеют случаи нарушения химического равновесия вследствие уменьшения концентрации какого-либо из веществ, участвующих в равновесии; изменение давления и температуры. Эти нарушения равновесия регламентируются принципом Ле-Шателье: если на систему, находящуюся в равновесии оказать воздействие, то в результате протекающих в ней процессов, равновесие сместится в таком направлении, что оказанное воздействие уменьшится.
60. Правило фаз Гиббса. Для любой системы, находящейся в равновесии сумма числа фаз (Р) и числа возможных состояний системы (V) больше числа компонентов (С) на 2: P + V = C+2
61. Растворы. Процесс растворения. Раствором называется твёрдое, газообразное или жидкая гомогенная система, состоящая их двух или более компонентов, относительно количества которых могут изменяться в широких пределах. Наиболее важный вид растворов – жидкий. Всякий раствор состоит из растворённых веществ и растворителя, т.е. среды, в которой эти вещества равномерно распределены в виде молекул или ионов. Обычно растворителем считают тот компонент, который в чистом виде существует в том же агрегатном состоянии, что и полученный раствор.
Однородность растворов делает их очень сходными с химическими соединениями.
Отличия раствора от химических соединений состоит в том, что состав раствора может меняться в очень широких пределах. Кроме того в свойствах раствора можно обнаружить многие свойства его отдельных компонентов, чего не наблюдается в случаях химических соединений.
Непостоянство состава растворов приближает их к механическим смесям, но от них они резко отличаются своей однородностью. Растворы занимают промежуточное положение между механическими смесями и химическими соединениями.
Отделение молекул от поверхности кристалла при растворении вызывается с одной стороны собственными тепловыми колебаниями молекул, а с другой стороны – притяжением молекул растворителем.
Раствор, находящийся в равновесии с растворенным веществом называется насыщенным раствором.
62. Способы выражения состава раствора. а) Массовая доля: ω=m 1 /(m 1 +m 2) * 100% где m 1 – растворенное вещество; m 1 +m 2 – масса раствора; m 2 – масса растворителя;
б) Мольная доля N= ν 1 /ν 1 +ν 2 – это отношение количества молей растворённого вещества к сумме количества всех веществ, составляющих раствор;
в) Молярная концентрация C = V 1 / m 2 – отношение количества вещества, содержащегося в растворе, к объёму раствора (моль/л);
г) Моляйная концентрация C = V э1 /V – отношение количества вещества, содержащегося в растворе, к массе растворителя (моль \ кг);
д) Молярная концентрация эквивалента – это отношение количества вещества эквивалента, содержащегося в растворе, к объёму этого раствора (моль/л).
63.Растворимость, Закон Генри. Растворимостью называют способность вещества растворяться в том или ином растворителе. Мерой растворимости вещества служит при данных условиях содержание его в насыщенном растворе. Однако, обычно, вещества состоящие из полярных молекул, и вещества с ионным типом связи лучше растворяются в полярных растворителях (вода, спирт, аммиак), а неполярные вещества – в неполярных растворителях (бензол и т.д.). Если растворение твёрдого вещества в жидкости сопровождается поглощение теплоты, то увеличение температуры приводит к повышению растворимости вещества.
При растворении твёрдых тел объём системы обычно изменяется незначительно. По этому растворимость твёрдых тел в жидкостях не зависит от давления.
Закон Генри: масса газа, растворяющегося при постоянной температуре в данном объёме жидкости прямо пропорциональна парциальному давлению газа.С=кр, где С – массо-объемная концентрация, р – парциальное давление газа, к – коэффициент Генри.
Следствие из закона Генри:
а) Объём газа, растворённого при постоянной температуре в данном объёме жидкости не зависит от его парциального давления.
б) Если над жидкостью находится смесь газов, то растворение каждого из них определено парциальным давлением.
64. Закон распределения. Экстракция. Закон распределения: вещество, способное растворяться в 2-х несмешивающихся растворителях распределяется между ними так, что отношение его концентраций в этих растворителях при постоянной температуре остаётся постоянным, независимо от общего количества растворённого вещества.
Экстракция – способ извлечения вещества из раствора метод с помощью подходящего растворителя (экстрагента). Для извлечения из раствора применяются растворители, не смешивающиеся с этим раствором, но в которых вещество растворяется лучше, чем в первом растворителе
65. Осмос. Закон Вант-Гоффа. Осмос- односторонняя диффузия молекул через полупроницаемую мембрану.
При измерении осмотического давления различных растворов было установлено, что величина осмотического давления зависит от концентрации раствора и от его температуры, но не зависит от природы растворяющихся веществ и растворителя.
P=CRT - закон Вант-Гоффа
где P- осмотическое давление раствора (Па), C – молярность, R – универсальная газовая постоянная, T – абсолютная температура
66. Давление пара раствора. Закон Рауля. При данной температуре давление пара над жидкостью – величина постоянная. При растворении в жидкости какого-либо вещества давление насыщенного пара в этой жидкости понижается.
Пар, находящийся в равновесии со своей жидкостью, называется насыщенным.
Давление насыщенного пара зависит от природы жидкости и температуры, но не зависит от объёма сосуда, в котором находится пар.
Таким образом, давление насыщенного пара растворителя над раствором всегда ниже чем над чистым растворителем при той же температура.
Разность между давлением насыщенного пара над чистым растворителем и над раствором, называют понижением пара раствора, а отношение понижения давления пара раствора к давлению насыщенного пара над чистым растворителем называется относительным понижением давления пара над раствором.
Закон Рауля: относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворённого вещества.
Явление понижения давления насыщенного пара над раствором вытекает из принципа Ле-Шателье.
67. Водные растворы электролитов. Теория электролитической диссоциации. а) Диссоциация солей, т.е. кристаллов с ионной структурой.
б) Диссоциация при растворении кислот, т.е. полярных молекул.
Теория электролитической диссоциации.
Электролитическая диссоциация- процесс распада электролита на ионы при его растворении или плавлении.
Классическая теория электролитической диссоциации была создана С. Аррениусом и В. Оствальдом в 1887 году. Аррениус придерживался физической теории растворов, не учитывал взаимодействие электролита с водой и считал, что в растворах находятся свободные ионы. Русские химики И. А. Каблуков и В. А. Кистяковский применили для объяснения электролитической диссоциации химическую теорию растворов Д. И. Менделеева и доказали, что при растворении электролита происходит его химическое взаимодействие с водой, в результате которого электролит диссоциирует на ионы.
Классическая теория электролитической диссоциации основана на предположении о неполной диссоциации растворённого вещества, характеризуемой степенью диссоциации α, т.е. долей распавшихся молекул электролита. Динамическое равновесие между недиссоциированными молекулами и ионами описывается законом действующих масс.
68. Сильные и слабые электролиты. Степень диссоциации. Степенью диссоциации электролита называется отношение числа молекул, распавшихся в данном растворе на ионы к общему числу молекул данного вещества в растворе.
Электролиты, степень диссоциации которых стремится к 1 называются сильными: NaCl, NaOH, HCl.
Электролиты, степень диссоциации которых стремится к 0 – называются слабыми: H 2 O, H 2 CO 2 , NH 4 OH.
69. Константа диссоциации. Закон разбавления Оствальда. К равновесиям, которые устанавливаются при диссоциации слабого электролита возможно применить законы, справедливые для химического равновесия.
Константа равновесия, отвечающая диссоциации слабого электролита, называется константой диссоциации.
Значение константы равновесия зависит от природы электролита и растворителя, от температуры, но не зависит от концентрации раствора. Эта величина характеризует способность данной кислоты, основания или соли распадаться на ионы. Чем выше величина константы равновесия, тем легче электролит диссоциирует на ионы.
Закон Оствальда – степень диссоциации возрастает по мере разбавления электролита.
70. Состояние сильных электролитов в растворе. Активность. Ионная сила. Для оценки состояния ионов в растворах сильных электролитов пользуются величиной, называемой активностью. Под активностью иона понимают ту эффективную условную концентрацию его, в соответствии с которой он действует при химических реакциях:
где а – активность иона, с- концентрация иона, f – коэффициент активности.
Для разбавления растворов справедливо выражение, которое связывает коэффициент активности и величину ионной силы раствора.
lgF= - 0.5Z 2 корень квадратный I
Если пользоваться значениями активностей, то законы химического равновесия можно применять и для растворов сильных электролитов.
71. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации. Кислоты способны взаимодействовать с основаниями. При этом образуются соли и вода.
Теория электролитической диссоциации определяет кислоты, как электролиты, диссоциирующие с образованием положительно заряженных ионов водорода.
Аналогично, основания определяют как электролиты, диссоциирующие с образованием отрицательно заряженного гидроксид-иона.
Соли: ионы гидроксида и водорода не образуются. Их рассматривают как электролиты, диссоциирующие с образованием положительно заряженных ионов, отличных от ионов водорода и отрицательно заряженных ионов, отличных от гидроксид-иона.
Химическим равновесием называется такое состояние обратимой химической реакции
aA + b B = c C + d D,
при котором с течением времени не происходит изменения концентраций реагирующих веществ в реакционной смеси. Состояние химического равновесия характеризуется константой химического равновесия :
где C i – концентрации компонентов в равновесной идеальной смеси.
Константа равновесия может быть выражена также через равновесные мольные доли X i компонентов:
Для реакций, протекающих в газовой фазе, константу равновесия удобно выражать через равновесные парциальные давления P i компонентов:
Для идеальных газов P i = C i RT и P i = X i P , где P – общее давление, поэтому K P , K C и K X связаны следующим соотношением:
K P = K C (RT) c+d–a–b = K X P c+d–a–b . (9.4)
Константа равновесия связана с r G o химической реакции:
![]() (9.5)
(9.5)
![]() (9.6)
(9.6)
Изменение r G или r F в химической реакции при заданных (не обязательно равновесных) парциальных давлениях P i или концентрациях C i компонентов можно рассчитать по уравнению изотермы химической реакции (изотермы Вант-Гоффа ):
 . (9.7)
. (9.7)
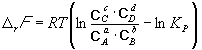 . (9.8)
. (9.8)
Согласно принципу Ле Шателье , если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится так, чтобы уменьшить эффект внешнего воздействия. Так, повышение давления сдвигает равновесие в сторону уменьшения количества молекул газа. Добавление в равновесную смесь какого-либо компонента реакции сдвигает равновесие в сторону уменьшения количества этого компонента. Повышение (или понижение) температуры сдвигает равновесие в сторону реакции, протекающей с поглощением (выделением) теплоты.
Количественно зависимость константы равновесия от температуры описывается уравнением изобары химической реакции (изобары Вант-Гоффа )
![]() (9.9)
(9.9)
и изохоры химической реакции (изохоры Вант-Гоффа )
![]() . (9.10)
. (9.10)
Интегрирование уравнения (9.9) в предположении, что r H реакции не зависит от температуры (что справедливо в узких интервалах температур), дает:
![]() (9.11)
(9.11)
![]() (9.12)
(9.12)
где C – константа интегрирования. Таким образом, зависимость ln K P от 1/Т должна быть линейной, а наклон прямой равен – r H /R .
Интегрирование в пределах K 1 , K 2 , и T 1, T 2 дает:
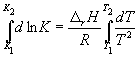 (9.13)
(9.13)
 (9.14)
(9.14)
По этому уравнению, зная константы равновесия при двух разных температурах, можно рассчитать r H реакции. Соответственно, зная r H реакции и константу равновесия при одной температуре, можно рассчитать константу равновесия при другой температуре.
ПРИМЕРЫ
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K. f G o для CO(г) и CH 3 OH(г) при 500 К равны –155.41 кДж. моль –1 и –134.20 кДж. моль –1 соответственно.
Решение. G o реакции:
r G o = f G o (CH 3 OH) – f G o (CO) = –134.20 – (–155.41) = 21.21 кДж. моль –1 .
![]() = 6.09 10 –3 .
= 6.09 10 –3 .
Пример 9-2. Константа равновесия реакции
равна K P = 1.64 10 –4 при 400 o C. Какое общее давление необходимо приложить к эквимолярной смеси N 2 и H 2 , чтобы 10% N 2 превратилось в NH 3 ? Газы считать идеальными.
Решение. Пусть прореагировало моль N 2 . Тогда
| N 2 (г) | + | 3H 2 (г) | = | 2NH 3 (г) | |
| Исходное количество | 1 | 1 | |||
| Равновесное количество | 1– | 1–3 | 2 (Всего: 2–2) | ||
| Равновесная мольная доля: |
Следовательно, K
X = 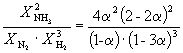 и K P = K X . P
–2
=
и K P = K X . P
–2
= 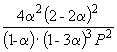 .
.
Подставляя = 0.1 в полученную формулу, имеем
1.64 10 –4 = , откуда P
= 51.2 атм.
, откуда P
= 51.2 атм.
Пример 9-3. Константа равновесия реакции
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K равна K P = 6.09 10 –3 . Реакционная смесь, состоящая из 1 моль CO, 2 моль H 2 и 1 моль инертного газа (N 2) нагрета до 500 K и общего давления 100 атм. Рассчитать состав равновесной смеси.
Решение. Пусть прореагировало моль CO. Тогда
| CO(г) | + | 2H 2 (г) | = | CH 3 OH(г) | |
| Исходное количество: | 1 | 2 | 0 | ||
| Равновесное количество: | 1– | 2–2 | |||
| Всего в равновесной смеси: | 3–2 моль компонентов + 1 моль N 2 = 4–2 моль | ||||
| Равновесная мольная доля | |||||
Следовательно, K
X = 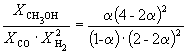 и K P = K X . P –2
=
и K P = K X . P –2
= ![]() .
.
Таким образом, 6.09 10 –3
= ![]() .
.
Решая это уравнение, получаем = 0.732. Соответственно, мольные доли веществ в равновесной смеси равны: = 0.288, = 0.106, = 0.212 и = 0.394.
Пример 9-4. Для реакции
N 2 (г) + 3H 2 (г) = 2NH 3 (г)
при 298 К K P = 6.0 10 5 , а f H o (NH 3) = –46.1 кДж. моль –1 . Оценить значение константы равновесия при 500 К.
Решение. Стандартная мольная энтальпия реакции равна
r H o = 2 f H o (NH 3) = –92.2 кДж. моль –1 .
Согласно уравнению (9.14),  =
=
Ln (6.0 10 5) + ![]() = –1.73, откуда K
2 =
0.18.
= –1.73, откуда K
2 =
0.18.
Отметим, что константа равновесия экзотермической реакции уменьшается с ростом температуры, что соответствует принципу Ле Шателье.
ЗАДАЧИ
- При 1273 К и общем давлении 30 атм в равновесной смеси
- При 2000 o C и общем давлении 1 атм 2% воды диссоциировано на водород и кислород. Рассчитать константу равновесия реакции
- Константа равновесия реакции
- Константа равновесия реакции
- Сосуд объемом 3 л, содержащий 1.79 10 –2 моль I 2 , нагрели до 973 K. Давление в сосуде при равновесии оказалось равно 0.49 атм. Считая газы идеальными, рассчитать константу равновесия при 973 K для реакции
- Для реакции
- Для реакции
- Сосуд объемом 1 л, содержащий 0.341 моль PCl 5 и 0.233 моль N 2 , нагрели до 250 o C. Общее давление в сосуде при равновесии оказалось равно 29.33 атм. Считая все газы идеальными, рассчитать константу равновесия при 250 o C для протекающей в сосуде реакции
- Константа равновесия реакции
- При 25 o C f G o (NH 3) = –16.5 кДж. моль –1 . Рассчитать r G реакции образования NH 3 при парциальных давлениях N 2 , H 2 и NH 3 , равных 3 атм, 1 атм и 4 атм соответственно. В какую сторону реакция будет идти самопроизвольно при этих условиях?
- Экзотермическая реакция
- Константа равновесия газофазной реакции изомеризации борнеола (C 10 H 17 OH) в изоборнеол равна 0.106 при 503 K. Смесь 7.5 г борнеола и 14.0 г изоборнеола поместили в сосуд объемом 5 л и выдерживали при 503 K до достижения равновесия. Рассчитать мольные доли и массы борнеола и изоборнеола в равновесной смеси.
- Равновесие в реакции
- Рассчитать общее давление, которое необходимо приложить к смеси 3 частей H 2 и 1 части N 2 , чтобы получить равновесную смесь, содержащую 10% NH 3 по объему при 400 o C. Константа равновесия для реакции
- При 250 o C и общем давлении 1 атм PCl 5 диссоциирован на 80% по реакции
- При 2000 o C для реакции
- Рассчитать стандартную энтальпию реакции, для
которой константа равновесия
а) увеличивается в 2 раза, б) уменьшается в 2 раза при изменении температуры от 298 К до 308 К. - Зависимость константы равновесия реакции 2C 3 H 6 (г) = C 2 H 4 (г) + C 4 H 8 (г) от температуры между 300 К и 600 К описывается уравнением
CO 2 (г) + C(тв) = 2CO(г)
содержится 17% (по объему) CO 2 . Сколько процентов CO 2 будет содержаться в газе при общем давлении 20 атм? При каком давлении в газе будет содержаться 25% CO 2 ?
H 2 O(г) = H 2 (г) + 1/2O 2 (г) при этих условиях.
CO(г) + H 2 O(г) = CO 2 (г) + H 2 (г)
при 500 o C равна K p = 5.5. Смесь, состоящая из 1 моль CO и 5 моль H 2 O, нагрели до этой температуры. Рассчитать мольную долю H 2 O в равновесной смеси.
N 2 O 4 (г) = 2NO 2 (г)
при 25 o C равна K p = 0.143. Рассчитать давление, которое установится в сосуде объемом 1 л, в который поместили 1 г N 2 O 4 при этой температуре.
I 2 (г) = 2I (г).
при 250 o C r G o = –2508 Дж. моль –1 . При каком общем давлении степень превращения PCl 5 в PCl 3 и Cl 2 при 250 o C составит 30%?
2HI(г) = H 2 (г) + I 2 (г)
константа равновесия K P = 1.83 10 –2 при 698.6 К. Сколько граммов HI образуется при нагревании до этой температуры 10 г I 2 и 0.2 г H 2 в трехлитровом сосуде? Чему равны парциальные давления H 2 , I 2 и HI?
PCl 5 (г) = PCl 3 (г) + Cl 2 (г)
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K равна K P = 6.09 10 –3 . Рассчитать общее давление, необходимое для получения метанола с 90% выходом, если CO и H 2 взяты в соотношении 1: 2.
CO(г) + 2H 2 (г) = CH 3 OH(г)
находится в равновесии при 500 K и 10 бар. Если газы идеальные, как повлияют на выход метанола следующие факторы: а) повышение T ; б) повышение P ; в) добавление инертного газа при V = const; г) добавление инертного газа при P = const; д) добавление H 2 при P = const?
2NOCl(г) = 2NO(г) + Cl 2 (г)
устанавливается при 227 o C и общем давлении 1.0 бар, когда парциальное давление NOCl равно 0.64 бар (изначально присутствовал только NOCl). Рассчитать r G o для реакции. При каком общем давлении парциальное давление Cl 2 будет равно 0.10 бар?
N 2 (г) + 3H 2 (г) = 2NH 3 (г)
при 400 o C равна K = 1.60 10 –4 .
PCl 5 (г) = PCl 3 (г) + Cl 2 (г).
Чему будет равна степень диссоциации PCl 5 , если в систему добавить N 2 , чтобы парциальное давление азота было равно 0.9 атм? Общее давление поддерживается равным 1 атм.
N 2 (г) + O 2 (г) = 2NO(г)
K p = 2.5 10 –3 . В равновесной смеси N 2 , O 2 , NO и инертного газа при общем давлении 1 бар содержится 80% (по объему) N 2 и 16% O 2 . Сколько процентов по объему составляет NO? Чему равно парциальное давление инертного газа?
ln K = –1.04 –1088 /T +1.51 10 5 /T 2 .
При некоторой температуре энтальпийный и энтропийный факторы реакции могут уравновешиваться, тогда устанавливается состояние равновесия, которому отвечает равенство ∆ r G Т = 0. В этом состоянии свободная энергия системы минимальна, а возможность протекания прямой и обратной реакции равновероятна, при этом в единицу времени получается столько же продуктов реакции, сколько их расходуется в обратной реакции образования исходных веществ. В таких условиях парциальные давления и концентрации всех компонентов реакции будут постоянными во времени и во всех точках системы и называются равновесными давлениями и концентрациями.
Если реакция протекает в изохорно-изотермических условиях, то условием химического равновесия является равенство Δ r F Т = 0. Из уравнений (1.12) и (1.15) следует, что при равновесии химической реакции a A(г)+b B(г)+ d D(к) ↔ e E(г)+ f F(г)
∆ r G 0 Т = - RT ln(p e E равн p f F равн /p a A равн p b B равн) . (2.1)
Если данная гетерогенная реакция с участием газообразных компонентов протекает при постоянном объеме, то
∆ r F 0 Т = - RT ln(c e E равн c f F равн /c a A равн c b B равн) . (2.2)
Если реакция a A(р)+b B(р)+d D(к)=e E(р)+f F(р) протекает в идеальном растворе, то из (1.12а) следует:
∆ r G 0 Т =∆ r F 0 Т = - RT ln(c e E равн c f F равн /c a A равн c b B равн) . (2.3)
Поскольку величины ∆ r F 0 Т и ∆ r G 0 Т для данной температуры есть величины постоянные, то эти уравнения справедливы, если под знаком логарифма находятся постоянные для данной температуры выражения, получившие название констант равновесия К с и К р :
К с = (c e E равн c f F равн /c a A равн c b B равн) (2.4)
К р = (p e E равн p f F равн /p a A равн p b B равн) . (2.5)
Уравнения (2.4) и (2.5) являются математическим выражением закона действующих масс.
Для реакций с газообразными компонентами связь между К р и К с выражается уравнением: К р = К с (RT ) ∆ν , (2.6) где ∆ν =(e+f-a-b ) – изменение числа молей газов в результате реакции, а R = 0,082 атм . л . моль -1. К -1 . Следует обратить внимание, что в выражение для К с и К р не входят компоненты в более конденсированном состоянии (например, вещество D в кристаллическом состоянии).
Константу равновесия К р можно выразить также через равновесные количества молей газообразных компонентов n i равн и общее давление P 0 , при котором проводят изобарно-изотермическую реакцию. Учитывая, что парциальное давление i -ого компонента пропорционально молярной доле этого компонента p i = (n i /Σn i )P 0 , из уравнения (2.5) получаем:
К р =(p e E равн p f F равн /p a A равн p b B равн)=(n e E равн n f F равн /n a A равн n b B равн)(P 0 /Σn i ) ∆ν (2.6)
где Σn i = (n E равн + n F равн + n A равн + n B равн)–сумма равновесных молей всех газообразных компонентов.
Объединяя уравнения (2.1), (2.2), (2.3) с уравнениями (2.4) и (2.5) получаем выражения, часто применяемые для расчетов:
∆ r G 0 Т = - RT lnК р и(2.7)
∆ r F 0 Т = - RT lnК с для газофазныхреакций. (2.8)
∆ r G 0 Т =- RT lnК с для реакций в конденсированных системах. (2.7а)
Таким образом, рассчитав энергию Гиббса реакции для заданной температуры, можно по данным формулам рассчитать К с и К р приэтой температуре. Чем больше величина константы равновесия в данных условиях, тем больше значения равновесных концентраций продуктов реакции, следовательно, тем выше выход продуктов реакции. Под выходом продукта реакции понимают отношение количества (или массы) продукта реакции, которое образовалось в данных условиях, к максимально возможному (теоретически) количеству (или массе) этого продукта при условии полного превращения какого-либо исходного вещества в продукт реакции. Очевидно, что полное (100%) превращение исходного вещества в продукт с термодинамических позиций невозможно, так как при этом константа равновесия становится бесконечно большой.
Под степенью превращения исходного вещества понимают отношение количества (или массы) исходного вещества, которое прореагировало в данных условиях, к начальному количеству (или массе) этого вещества. Если выход продукта стремится к единице (100%), то степень превращения исходного вещества также приближается к единице (100%).
Значения К р и К с при данной температуре не зависят от величин парциальных давлений и концентраций компонентов, а также общего давления в системе, но зависят от температуры. Зависимость константы равновесия от температуры можно выразить в дифференциальной форме:
(d ln K p / dT ) = ∆ r H 0 /(RT 2) , (2.9) где ∆ r Н 0 - стандартная энтальпия реакции, которую в первом приближении считают не зависящей от температуры. Как видно из (2.9), с ростом температуры константа равновесия экзотермической реакции уменьшается, а константа равновесия эндотермической реакции увеличивается.
При интегрировании выражения (2.9) с учетом указанного приближения получаем (при Т 2 > Т 1) формулу
ln(K 2 /K 1) = (∆ r H 0 /R )(1/T 1 – 1/T 2) , (2.10)
из которой следует, что чем больше абсолютная величина теплового эффекта реакции, тем сильнее изменяется значение константы равновесия с изменением температуры. Эту формулу можно использовать также для расчета величины К равн при какой-либо Т 3 , если известны значения К 2 и К 1 при температурах Т 2 и Т 1 .
Пример 10. Запишите выражение дляК с и К р и рассчитайте К р и К с реакции С(к) + СО 2 (г) = 2СО(г) при 298 К и при 1000 К. Сделайте вывод по полученным значениям о выходе продукта реакции при данных температурах и о влиянии температуры на величину константы равновесия.
Решение. Запишем выражения для констант равновесия данной реакции, принимая во внимание, что реакция гетерогенная и вещество графит С(к) находится в твердом состоянии:
К р = p 2 CO равн /p CO 2равн; К с = с 2 CO равн /с CO 2равн
Из уравнения (2.7) имеем K p =exp(-∆G 0 Т /RT) . Используя результаты примера 5, рассчитаем К р для 298 К и 1000 К:
К р 298 = exp(-120 . 10 3 /8,31 . 298)= ехр(-48,5) << 1;
K p 1000 =exp(+316/8,31 . 1000)= ехр(0,038) = 1,039.
По формуле (2.6) находим К с = К р /(RT ) ∆ν = 1,039/0,082 . 1000 = 0,013, так как ∆ν = 2-1=1. По полученным данным можно сделать вывод, что при 298 К константа равновесия К р стремится к нулю, что говорит о том, что в равновесной смеси практически отсутствуют продукты реакции и равновесие реакции сильно смещено в сторону исходных веществ. С ростом температуры величина константы равновесия возрастает (реакция эндотермическая) и при 1000 К К р уже больше 1, то есть в равновесной смеси начинают преобладать продукты реакции, их выход растет с ростом Т.
Пример 11. Для некоторой реакции А(г) = 2В(г), идущей при постоянных давлении и температуре, константа равновесия К р равна 0,02 при 400 К и 4,0 при 600 К. Определите по этим данным ∆ r H 0 298 , ∆ r S 0 298 и ∆ r G 0 298 этой реакции, а также К р при 800 К.
Решение. Пренебрегая зависимостью ∆ r H 0 и ∆ r S 0 от температуры и используя выражения (1.14) и (2.7) составим систему из двух уравнений с двумя неизвестными (T 1 =400 K, T 2 =600 K):
∆ r G 0 Т 1 =∆ r H 0 298 –T 1 ∆ r S 0 298 = -RT 1 lnК р 1 или x – 400y = -8,31.400 ln2 . 10 -2
∆ r G 0 Т 2 =∆ r H 0 298 –T 2 ∆ r S 0 298 = -RT 2 lnК р 2 или x – 600y = -8,31 . 600 ln4
Откуда х = ∆ r H 0 298 = 52833(Дж)= 52,833 кДж; y =∆ r S 0 298 =99,575Дж/К.
Значение К р при 800 К рассчитаем по формуле (2.10). Имеем:
ln(K 800 /K 400) = ln(K 800 /0,02)= (52833/8,31)(1/400 -1/800) = 7,95. Откуда К 800 = 56,55.
Пример 10. Определите температуру, при которой в реакции СаСО 3 (к) = СаО(к) + СО 2 (г) равновесное парциальное давление СО 2 р СО2 = 10 4 Па.
Решение. Для данной гетерогенной реакции запишем выражение для константы равновесия: К р = р СО2 , то есть константа равновесия равна относительному парциальному давлению СО 2 при данной температуре. Для искомой температуры К р =р СО2 = 10 4 /10 5 =0,1.Пренебрегая зависимостью ∆ r H 0 и ∆ r S 0 от температуры, воспользуемся формулами (1.14) и (2.7) и приравняем друг другу два выражения для ∆ r G 0 Т : ∆ r G 0 Т = ∆ r H 0 298 –T ∆ r S 0 298 = -RT lnК р . Значения ∆ r H 0 298 и ∆ r S 0 298 определяем, как рассмотрено выше, по табличным данным: ∆rH 0 298 =178,1 кДж; ∆rS 0 298 =160,5 Дж. Имеем:
178,1 . 10 3 –Т . 160,5
∆rG 0 Т = -8,31Т ln0,1
Решая полученную систему уравнений относительно Т, находим Т =991К
Константа химического равновесия - характеристика химической реакции, по значению которой можно судить о направлении процесса при исходном соотношении концентраций реагирующих веществ, о максимально возможном выходе продукта реакции при тех или иных условиях.
Константа химического равновесия определяется по закону действующих масс . Ее значения находят расчетно или на основании экспериментальных данных. Константа химического равновесия зависит от природы реагентов и от температуры.
Константа равновесия и энергия Гиббса
Константа равновесия ~K связана со свободной энергией Гиббса ~\Delta G следующим образом:
~\Delta G=-RT\cdot\ln K.Приведенное уравнение позволяет по величине ΔG° вычислить К, а затем и равновесные концентрации (парциальные давления) реагентов.
Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры (если выразить отсюда константу, то температура будет в показателе степени). Для эндотермических процессов повышение температуры отвечает увеличению константы равновесия, для экзотермических - ее уменьшению. От давления константа равновесия не зависит, кроме случаев очень большого давления (от 100 Па).
Зависимость константы равновесия от энтальпийного и энтропийного факторов свидетельствует о влиянии на нее природы реагентов.
Константа равновесия и скорость реакции
Можно выразить константу равновесия через скорость реакции. При этом константа равновесия определяется как
~K=\frac{k_1}{k_{-1}},где ~k_1 - константа скорости прямой реакции, ~k_{-1} - константа скорости обратной реакции.
Количественная характеристика, показывающая направление реакции и смещение концентрации веществ, называется константой равновесия химической реакции. Константа равновесия зависит от температуры и природы реагентов.
Обратимые и необратимые реакции
Все реакции можно разделить на два типа:
- обратимые , одновременно протекающие в двух взаимно противоположных направлениях;
- необратимые , протекающие в одном направлении с полным расходом хотя бы одного исходного вещества.
При необратимых реакциях обычно образуются нерастворимые вещества в виде осадка или газа. К таким реакциям относятся:
- горение:
C 2 H 5 OH + 3O 2 → 2CO 2 + H 2 O;
- разложение:
2KMnO 4 → K 2 MnO 4 + MnO 2 + H 2 O;
- присоединение с образованием осадка или газа:
BaCl 2 + Na 2 SO 4 → BaSO 4 ↓ + 2NaCl.

Рис. 1. Образование осадка BaSO 4 .
Обратимые реакции возможны только в определённых неизменных условиях. Исходные вещества дают новое вещество, которое тут же распадается на составные части и собирается вновь. Например, в результате реакции 2NO + O 2 ↔ 2NO 2 оксид азота (IV) легко разлагается на оксид азота (II) и кислород.
Равновесие
Через определённое время скорость обратимой реакции замедляется. Достигается химическое равновесие - состояние, при котором не происходит изменения концентрации исходных веществ и продуктов реакции с течением времени, так как скорость прямой и обратной реакций уравниваются. Равновесие возможно только в гомогенных системах, то есть все реагирующие вещества являются либо жидкостями, либо газами.
Рассмотрим химическое равновесие на примере реакции взаимодействия водорода с йодом:
- прямая реакция -
H 2 + I 2 ↔ 2HI;
- обратная реакция -
2HI ↔ H 2 + I 2 .
Как только смешиваются два реагента - водород и йод - йодоводорода ещё не существует, так как простые вещества только вступают в реакцию. Большое количество исходных веществ активно реагируют друг с другом, поэтому скорость прямой реакции будет максимальной. При этом обратная реакция не протекает, и скорость её равна нулю.
Скорость прямой реакции можно выразить графически:
ν пр = k пр ∙ ∙ ,
где k пр - константа скорости прямой реакции.
Со временем реагенты расходуются, их концентрация снижается. Соответственно, скорость прямой реакции уменьшается. Одновременно с этим увеличивается концентрация нового вещества - йодоводорода. При накоплении он начинает разлагаться, и скорость обратной реакции повышается. Её можно выразить как
ν обр = k обр ∙ 2 .
Йодоводород в квадрате, так как коэффициент молекулы равен двум.
В определённый момент скорости прямой и обратной реакции уравниваются. Наступает состояние химического равновесия.

Рис. 2. График зависимости скорости реакции от времени.
Равновесие можно сместить либо в сторону исходных веществ, либо в сторону продуктов реакции. Смещение под воздействием внешних факторов называется принципом Ле Шателье. На равновесие влияют температура, давление, концентрация одного из веществ.
Расчёт константы
В состоянии равновесия обе реакции идут, но при этом концентрации веществ находятся в равновесии (образуются равновесные концентрации), так как уравновешенны скорости (ν пр = ν обр).
Химическое равновесие характеризуется константой химического равновесия, которая выражается сводной формулой:
K p = k пр / k обр = const.
Константы скорости реакции можно выразить через соотношение скорости реакции. Возьмём условное уравнение обратной реакции:
aA + bB ↔ cC + dD.
Тогда скорости прямой и обратной реакции будут равны:
- ν пр = k пр ∙ [A] p a ∙ [B] p b
- ν обр = k обр ∙ [C] p c ∙ [D] p d .
Соответственно, если
ν пр = ν обр,
k пр ∙ [A] p a ∙ [B] p b = k обр ∙ [C] p c ∙ [D] p d .
Отсюда можно выразить соотношение констант:
k обр / k пр = [C] p c ∙ [D] p d / [A] p a ∙ [B] p b .
Это соотношение равно константе равновесия:
K p = [C] p c ∙ [D] p d / [A] p a ∙ [B] p b .

Рис. 3. Формула константы равновесия.
Величина показывает, во сколько раз скорость прямой реакции больше скорости обратной реакции.
Что мы узнали?
Реакции в зависимости от конечных продуктов классифицируются на обратимые и необратимые. Обратимые реакции протекают в обе стороны: исходные вещества образуют конечные продукты, которые разлагаются на исходные вещества. В ходе реакции скорости прямой и обратной реакций уравновешиваются. Такое состояние называется химическим равновесием. Оно может быть выражено как соотношение произведения равновесных концентраций продуктов реакции к произведению разновесных концентраций исходных веществ.
Тест по теме
Оценка доклада
Средняя оценка: 4.8 . Всего получено оценок: 193.
